تقنية كريسبر وآلية عملها في تحرير الجينات
تقنية كريسبر تعتمد على نظام بيولوجي موجود في البكتيريا للدفاع ضد الفيروسات. تستخدم هذه التقنية لإنشاء “مقص جيني” دقيق جدًا. يتعرف هذا المقص على مواقع محددة في الحمض النووي ويقوم بقصها. بعد عملية القص، تستطيع الخلية إصلاح الحمض النووي أو استبداله بجزء جديد. يعتبر هذا النظام ثورة في مجال الهندسة الوراثية.
آلية عمل كريسبر تعتمد على نوعين من الجزيئات: كريسبر نفسه وجزيء يسمى Cas9. كريسبر يعتبر كمرشد يقود Cas9 إلى الموقع المطلوب في الحمض النووي. عندما يصل Cas9 إلى هذا الموقع، يقوم بقطع الحمض النووي بدقة عالية. تستطيع الخلية بعد ذلك تصحيح الخطأ أو إدخال جزء جديد من الحمض النووي. هذه الدقة تجعل تقنية كريسبر أداة قوية لتحرير الجينات.
تطبيق تقنية كريسبر في تحرير الجينات يفتح آفاقًا جديدة في علاج الأمراض الوراثية، بما في ذلك أمراض القلب. يستطيع العلماء استخدام كريسبر لاستهداف وتعديل الجينات المسؤولة عن الأمراض الوراثية في القلب. هذا التعديل يمكن أن يمنع تطور المرض أو حتى يعالجه بالكامل. يعتبر هذا التوجه جزءًا من الطب الشخصي المتقدم.
لكن كريسبر ليست خالية من التحديات. تتطلب هذه التقنية دقة فائقة لضمان استهداف الموقع الصحيح في الحمض النووي. أي خطأ في هذه العملية قد يؤدي إلى عواقب غير متوقعة. لذلك، يعمل العلماء باستمرار على تحسين كفاءة ودقة هذه التقنية لتقليل المخاطر المحتملة وضمان النتائج المرجوة.
استخدامات تقنية كريسبر في علاج أمراض القلب
تقنية كريسبر تُستخدم على نطاق واسع في الأبحاث لعلاج أمراض القلب. تعتمد هذه الأبحاث على تعديل الجينات المسؤولة عن تطور المرض. يمكن للعلماء تصحيح الطفرات الجينية التي تسبب أمراض القلب الوراثية. هذا التصحيح يمنع تطور المرض ويعزز صحة القلب.
تستخدم تقنية كريسبر في علاج اعتلال عضلة القلب المتوسع. يعمل الباحثون على تعديل الجينات المسؤولة عن ضعف عضلة القلب. يهدف هذا التعديل إلى تحسين قدرة العضلة على ضخ الدم بفعالية. هذه الجهود تُعدّ خطوة نحو إيجاد علاج دائم للمرض.
تساهم تقنية كريسبر في تطوير علاجات جديدة لأمراض الشرايين التاجية. تستهدف الأبحاث الجينات المسؤولة عن تراكم الدهون في الشرايين. يقوم العلماء بتعديل هذه الجينات للحد من التراكم وتحسين تدفق الدم. يساعد هذا التعديل في تقليل خطر الإصابة بالنوبات القلبية.
تُستخدم كريسبر أيضًا في أبحاث علاج فشل القلب. يستهدف العلماء الجينات التي تؤدي إلى ضعف ضخ الدم وتراكم السوائل في الجسم. يقومون بتعديل هذه الجينات لتحسين وظيفة القلب وتقليل الأعراض. هذا النوع من العلاج قد يوفر حلاً طويل الأمد لمرضى فشل القلب.
تقنية كريسبر وعلاج اعتلال عضلة القلب الوراثي
تقنية كريسبر تُستخدم بشكل متزايد لعلاج اعتلال عضلة القلب الوراثي. يستهدف العلماء الجينات المسؤولة عن هذا المرض لإصلاحها. هذا الإصلاح يهدف إلى منع تدهور عضلة القلب وتحسين وظيفتها. يعد هذا التقدم خطوة هامة نحو علاج أكثر فعالية لاعتلال عضلة القلب.
يعمل الباحثون على استهداف الجينات المتحورة التي تسبب ضعف عضلة القلب الوراثي. يتم تعديل هذه الجينات باستخدام تقنية كريسبر لإعادة البرمجة الجينية للعضلة. هذه العملية تهدف إلى استعادة وظيفة العضلة الطبيعية ومنع تدهورها المستمر. يُعزز هذا التوجه إمكانيات العلاج الشخصي للمرضى.
تعتمد الدراسات الحديثة على تقنية كريسبر لتطوير نماذج جديدة لاعتلال عضلة القلب الوراثي. تستخدم هذه النماذج لدراسة تأثير تعديل الجينات على المدى الطويل. تهدف هذه الأبحاث إلى فهم كيفية تأثير التعديلات الجينية على تطور المرض وتحديد أفضل الطرق للعلاج. تساعد هذه الأبحاث في تحسين كفاءة التقنية ودقة العلاج.
رغم التفاؤل الكبير، تواجه تقنية كريسبر تحديات في علاج اعتلال عضلة القلب الوراثي. تشمل هذه التحديات التأكد من دقة التعديلات الجينية وضمان عدم تأثيرها على جينات أخرى. أي خطأ في التعديل يمكن أن يؤدي إلى عواقب غير مرغوب فيها. لذلك، يُجري العلماء أبحاثًا مكثفة لتحسين دقة هذه التقنية وضمان سلامتها.
تقنية كريسبر وإصلاح العيوب الجينية في القلب
تقنية كريسبر توفر أداة قوية لإصلاح العيوب الجينية التي تؤثر على القلب. يعتمد العلماء على هذه التقنية لتعديل الجينات المسؤولة عن تشوهات القلب الخلقية. يمكن للتعديلات الجينية التي تقوم بها كريسبر أن تصحح العيوب الوراثية وتحسن من وظائف القلب بشكل كبير.
تشوهات القلب الخلقية قد تنتج عن طفرات جينية معينة. تقنية كريسبر تمكن العلماء من استهداف هذه الطفرات بدقة عالية. يتم تعديل الجينات المتضررة لتصحيح الخلل الجيني، مما يساعد في الوقاية من مشاكل القلب الخطيرة. هذا التعديل يمكن أن يحدث قبل ولادة الطفل، مما يوفر فرصة لعلاج مبكر.
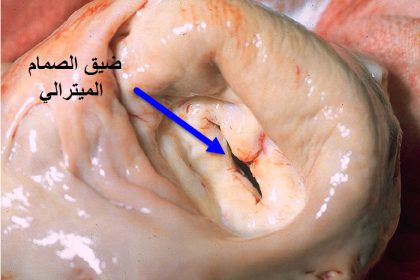
في الأبحاث المتقدمة، يجري العلماء تجارب على إصلاح عيوب صمامات القلب باستخدام كريسبر. تستهدف هذه التجارب الجينات المسؤولة عن تكون الصمامات بشكل غير طبيعي. يتم تعديل هذه الجينات لتحفيز نمو صمامات سليمة، مما يمكن أن يقلل من الحاجة إلى العمليات الجراحية لاحقًا في الحياة. هذه البحوث تمثل تقدمًا كبيرًا في مجال الطب الوقائي.
رغم الفوائد المحتملة، تواجه تقنية كريسبر تحديات كبيرة في إصلاح العيوب الجينية في القلب. تحتاج التعديلات الجينية إلى دقة عالية لتجنب التأثير على جينات أخرى. يعمل الباحثون على تحسين تقنيات استهداف الجينات وضمان سلامة العملية برمتها. تهدف هذه الجهود إلى تحقيق أقصى فائدة ممكنة من تقنية كريسبر مع تقليل المخاطر المحتملة.
تطبيقات تقنية كريسبر في علاج أمراض الشرايين التاجية
تقنية كريسبر تفتح آفاقًا جديدة في علاج أمراض الشرايين التاجية. يعمل العلماء على استخدام هذه التقنية لتعديل الجينات التي تسهم في تطور تصلب الشرايين. هذا التعديل يمكن أن يحد من تراكم الدهون ويقلل من خطر انسداد الشرايين.
تصلب الشرايين التاجية هو السبب الرئيسي للنوبات القلبية. تقنية كريسبر تمكن الباحثين من استهداف الجينات التي تسهم في تراكم الكوليسترول والدهون على جدران الشرايين. من خلال تعديل هذه الجينات، يمكن تقليل التراكم وتحسين تدفق الدم إلى القلب، مما يقلل من خطر الإصابة بالنوبات القلبية.
تُستخدم تقنية كريسبر أيضًا في الأبحاث المتعلقة بالتهابات الشرايين التاجية. يتم استهداف الجينات التي تسبب التهابات مزمنة تؤدي إلى تضيق الشرايين. تعديل هذه الجينات يمكن أن يحد من الالتهاب ويمنع تضيق الشرايين، مما يعزز من صحة القلب ويقلل من الحاجة إلى التدخلات الجراحية مثل عملية القلب المفتوح .
رغم التقدم الكبير في الأبحاث، تواجه تقنية كريسبر تحديات كبيرة في تطبيقها على علاج أمراض الشرايين التاجية. تتطلب هذه التطبيقات دقة عالية في استهداف الجينات وضمان عدم حدوث تأثيرات جانبية غير مرغوبة. يعمل العلماء على تطوير تقنيات جديدة لتحسين دقة وسلامة هذه التعديلات الجينية، مما يعزز من فرص نجاحها في المستقبل.
دور تقنية كريسبر في علاج الرجفان الأذيني
الرجفان الأذيني هو اضطراب شائع في ضربات القلب يمكن أن يؤدي إلى مضاعفات خطيرة. تقنية كريسبر تُستخدم الآن في الأبحاث لاستهداف الجينات التي تسهم في حدوث هذا الاضطراب. تهدف هذه الأبحاث إلى تعديل الجينات المسؤولة لتحسين استقرار ضربات القلب ومنع الرجفان.
يركز الباحثون على جينات معينة تتعلق بتنظيم النشاط الكهربائي في القلب. باستخدام تقنية كريسبر، يتم تعديل هذه الجينات لتحسين التواصل الكهربائي بين خلايا القلب. هذا التعديل يساعد في تنظيم ضربات القلب بشكل طبيعي، مما يقلل من حدوث الرجفان الأذيني ويعزز من صحة القلب العامة.
في الأبحاث السريرية، يجري العلماء تجارب على استخدام كريسبر لعلاج الحالات المتقدمة من الرجفان الأذيني. تستهدف هذه الأبحاث الجينات التي تؤثر على وظيفة الأذينين، حيث يتم تعديل هذه الجينات لتحسين وظيفتها وتقليل احتمالية حدوث الرجفان. النتائج الأولية مشجعة وتظهر إمكانية تحويل هذه الأبحاث إلى علاجات فعلية.
رغم التقدم الكبير، تحتاج تقنية كريسبر إلى المزيد من الدراسات لضمان فعاليتها وسلامتها في علاج الرجفان الأذيني. تتطلب هذه العملية دقة كبيرة لتجنب التأثير على جينات أخرى في القلب. يعمل الباحثون على تحسين تقنيات الاستهداف وزيادة فهمهم للجينات المرتبطة بالرجفان الأذيني لضمان تحقيق أفضل النتائج العلاجية الممكنة.
تقنية كريسبر وعلاج أمراض القلب الخلقية
تقنية كريسبر تُعد أداة واعدة في علاج أمراض القلب الخلقية. تستهدف هذه الأمراض التي تنشأ بسبب طفرات جينية تؤدي إلى تشوهات في بنية القلب. يعمل العلماء على استخدام كريسبر لتعديل الجينات المسؤولة عن هذه التشوهات، مما يساعد في إصلاح القلب ومنع تطور المضاعفات.
أمراض القلب الخلقية تشمل مجموعة متنوعة من التشوهات، مثل ثقب القلب أو ضيق الشرايين. تقنية كريسبر تتيح للباحثين تعديل الجينات التي تسهم في هذه التشوهات. يتم إصلاح الجينات المتضررة قبل أو بعد الولادة، مما يعزز فرص تحسين حياة المرضى وتقليل الحاجة إلى التدخلات الجراحية لاحقًا.
في الأبحاث الحديثة، تُستخدم تقنية كريسبر لتطوير علاجات مبتكرة تستهدف أمراض القلب الخلقية المعقدة. يعمل الباحثون على تعديل جينات معينة لتحفيز النمو السليم للأوعية الدموية والصمامات القلبية. هذه التعديلات تساعد في تصحيح التشوهات وتحسين وظيفة القلب بشكل عام، مما يقدم أملًا كبيرًا في تحسين نوعية حياة المرضى.
رغم الفوائد الكبيرة المحتملة، تتطلب تقنية كريسبر المزيد من الدراسات لضمان سلامتها وفعاليتها في علاج أمراض القلب الخلقية. يجب على الباحثين توخي الحذر لتجنب التأثيرات غير المرغوب فيها على جينات أخرى. تحسين تقنيات الاستهداف الجيني وفهم أعمق للآليات الجينية المرتبطة بأمراض القلب الخلقية سيساهمان في تحقيق نتائج علاجية أفضل.
التحديات والقيود في استخدام كريسبر لعلاج أمراض القلب
رغم الفوائد المحتملة الكبيرة لتقنية كريسبر في علاج أمراض القلب، تواجه هذه التقنية عدة تحديات وقيود. تتطلب هذه التحديات تحسينات مستمرة لضمان نجاح العلاج الجيني وتحقيق الأهداف المرجوة. الدقة في استهداف الجينات تمثل أحد أكبر التحديات التي تواجه العلماء.
الاستهداف غير الدقيق للجينات قد يؤدي إلى تعديل جينات أخرى بشكل غير مقصود. هذا التعديل غير المقصود يمكن أن يتسبب في حدوث مشاكل صحية جديدة، مما يزيد من تعقيد العلاج. تحسين تقنيات كريسبر لتحديد المواقع المستهدفة بدقة هو أمر ضروري لضمان سلامة المرضى وتقليل المخاطر.
من القيود الأخرى التي تواجه استخدام كريسبر في علاج أمراض القلب هو التحديات المتعلقة بإيصال الأدوات الجينية إلى خلايا القلب. تحتاج الأدوات الجينية إلى طرق فعالة للوصول إلى جميع الخلايا المستهدفة داخل القلب. تطوير طرق إيصال أكثر فعالية وأمانًا يعد من الأولويات الحالية في هذا المجال.
رغم هذه التحديات، تستمر الأبحاث في التقدم وتحقيق نتائج واعدة. يعمل العلماء على تحسين دقة تقنية كريسبر وتقليل المخاطر المرتبطة باستخدامها. التطورات المستمرة في هذا المجال قد تؤدي إلى تحويل هذه التقنية إلى أداة فعالة وآمنة لعلاج أمراض القلب في المستقبل. ومع ذلك، يجب على المجتمع الطبي الاستمرار في تقييم الفوائد والمخاطر بعناية لضمان تحقيق أقصى استفادة من هذه التكنولوجيا الحديثة.
الأبحاث الحالية حول كريسبر وعلاج أمراض القلب
الأبحاث الحالية حول تقنية كريسبر في علاج أمراض القلب تشهد تطورًا ملحوظًا. يركز العلماء على استكشاف إمكانيات استخدام هذه التقنية لتعديل الجينات المسؤولة عن الأمراض القلبية الوراثية. هذه الأبحاث تهدف إلى إيجاد حلول جديدة وفعالة لعلاج هذه الأمراض، مما قد يحدث تحولاً كبيرًا في مجال الطب القلبي.
أحد المجالات البحثية الرئيسية يتعلق بتطوير نماذج حيوانية لدراسة تأثير كريسبر على أمراض القلب. يستخدم الباحثون هذه النماذج لتقييم فعالية وسلامة التعديلات الجينية التي تُجرى باستخدام كريسبر. هذه الدراسات توفر معلومات قيمة تساعد في فهم كيفية استجابة القلب لهذه التعديلات على المستوى الجزيئي.
تتضمن الأبحاث الحالية أيضًا تجارب سريرية مبكرة تهدف إلى استخدام كريسبر لعلاج أمراض قلبية معينة لدى البشر. تُجرى هذه التجارب بحذر شديد لضمان سلامة المرضى ولتقييم النتائج المحتملة لهذه التقنية. تُظهر النتائج الأولية بعض الفوائد المحتملة، لكنها تشير أيضًا إلى الحاجة إلى مزيد من الدراسات قبل اعتمادها كعلاج روتيني.
بالإضافة إلى ذلك، يركز الباحثون على تحسين كفاءة وفعالية تقنية كريسبر. يسعون إلى تطوير أدوات أكثر دقة لتحديد المواقع الجينية المستهدفة وتجنب التأثيرات الجانبية غير المرغوبة. هذه التحسينات تهدف إلى زيادة فرص النجاح في العلاج الجيني وتقليل المخاطر المرتبطة به. بشكل عام، تبدو الأبحاث الحالية واعدة، ولكنها تشير إلى أن الطريق ما زال طويلاً قبل أن تصبح كريسبر علاجًا قياسيًا لأمراض القلب.
الآثار الجانبية المحتملة لتقنية كريسبر في علاج القلب
رغم الفوائد المحتملة لتقنية كريسبر في علاج أمراض القلب، توجد بعض الآثار الجانبية المحتملة التي تثير قلق الباحثين والأطباء. أحد هذه الآثار هو التعديل غير المقصود للجينات غير المستهدفة. عندما تقوم تقنية كريسبر بقص الحمض النووي، قد يحدث خطأ في التعرف على الموقع الصحيح، مما يؤدي إلى تعديل جينات أخرى غير مرتبطة بالمرض القلبي.
تعديل جينات غير مستهدفة يمكن أن يؤدي إلى مشاكل صحية جديدة. قد تتسبب هذه التعديلات غير المقصودة في ظهور أمراض أو اضطرابات جديدة لدى المريض. على سبيل المثال، قد تؤدي التعديلات إلى ضعف في جهاز المناعة أو إلى تطور خلايا سرطانية. لذلك، تعتبر هذه المشكلة أحد التحديات الكبيرة التي تواجه الباحثين عند استخدام كريسبر في العلاج الجيني.
بالإضافة إلى ذلك، قد تسبب تقنية كريسبر استجابة مناعية في جسم المريض. عندما تُدخل أدوات كريسبر إلى الجسم، قد يتعرف عليها الجهاز المناعي على أنها أجسام غريبة ويهاجمها. هذا الهجوم المناعي يمكن أن يقلل من فعالية العلاج أو يسبب التهابات وأضرار في الأنسجة القلبية. لذلك، يُجرى حاليًا العديد من الأبحاث لتطوير طرق لتقليل هذه الاستجابات المناعية.
أخيرًا، يجب أيضًا النظر في الآثار طويلة الأمد لتقنية كريسبر. لم يتم بعد فهم التأثيرات طويلة الأجل للتعديلات الجينية التي تُجرى باستخدام هذه التقنية بشكل كامل. قد تظهر بعض المشاكل الصحية بعد سنوات من العلاج، مما يجعل المتابعة الطويلة للمريض ضرورية. هذه المخاطر تتطلب اهتمامًا خاصًا من المجتمع الطبي لضمان أن فوائد العلاج الجيني تفوق مخاطره المحتملة.
أخلاقيات استخدام تقنية كريسبر في العلاج الجيني
تقنية كريسبر تُثير العديد من التساؤلات الأخلاقية عند استخدامها في العلاج الجيني، خاصة في أمراض القلب. واحدة من هذه القضايا تتعلق بالتلاعب في الجينات البشرية. التعديل الجيني، رغم فوائده المحتملة، يثير مخاوف بشأن إمكانية تغيير الصفات الوراثية للإنسان بشكل غير مرغوب فيه. هذا يثير تساؤلات حول الحدود التي يجب أن يلتزم بها العلماء في هذا المجال.
جانب آخر من الأخلاقيات يتعلق بالتمييز بين الجينات التي يُسمح بتعديلها وتلك التي لا يُسمح بها. قد يؤدي تعديل الجينات لعلاج أمراض القلب إلى فتح الباب أمام التلاعب الجيني لأغراض غير علاجية، مثل تحسين القدرات البدنية أو الذهنية. هذا النوع من التعديلات يُعتبر مثيرًا للجدل، ويواجه انتقادات واسعة من المجتمع الأخلاقي والعلمي.
القضايا الأخلاقية تشمل أيضًا الوصول العادل إلى تقنيات العلاج الجيني. تقنية كريسبر تعتبر متقدمة وتكلفتها مرتفعة، مما قد يؤدي إلى تمييز في الوصول إلى العلاج. قد يكون هذا العلاج متاحًا فقط للأغنياء، مما يعمق الفجوة الصحية بين الطبقات الاجتماعية المختلفة. يجب أن تعمل المجتمعات على ضمان توفير العلاج الجيني بشكل عادل للجميع.
أخيرًا، تأتي قضية الموافقة المستنيرة كجزء أساسي من الأخلاقيات الطبية. قبل إجراء أي تعديل جيني باستخدام كريسبر، يجب أن يكون المرضى على دراية كاملة بالمخاطر والفوائد المحتملة. هذا يتطلب تواصلًا شفافًا وصريحًا بين الأطباء والمرضى. يجب أن يكون لدى المرضى الحق في رفض أو قبول العلاج بناءً على فهم كامل للعواقب المحتملة.
مستقبل تقنية كريسبر في علاج أمراض القلب
مستقبل تقنية كريسبر في علاج أمراض القلب يبدو واعدًا، حيث تستمر الأبحاث في تطوير هذه التقنية وتحسينها. يعمل العلماء على زيادة دقة وكفاءة كريسبر لتجنب الآثار الجانبية وتحقيق نتائج أفضل في العلاج الجيني. هذه التحسينات قد تجعل من كريسبر أداة رئيسية في علاج العديد من الأمراض القلبية المعقدة.
تقنية كريسبر قد تفتح الباب أمام علاجات جديدة لأمراض القلب الوراثية التي لا يوجد لها علاج حاليًا. من خلال تعديل الجينات المسؤولة عن هذه الأمراض، يمكن أن يساعد كريسبر في الوقاية من تطور المرض أو حتى علاجه بشكل كامل. هذا التحول قد يغير مستقبل الطب القلبي بشكل جذري، مما يوفر حلولًا جديدة وفعالة للمرضى.
في المستقبل، قد تُستخدم تقنية كريسبر بشكل وقائي لتعديل الجينات في الأجنة أو قبل ظهور الأعراض المرضية. هذه المقاربة يمكن أن تمنع الأمراض القلبية الوراثية من الانتقال عبر الأجيال، مما يقلل من عبء هذه الأمراض على الأفراد والمجتمع. ومع ذلك، يتطلب هذا التطبيق دراسة دقيقة للأخلاقيات والتداعيات الاجتماعية المرتبطة به.
رغم التقدم المذهل، ما زال هناك الكثير من العمل الذي يجب القيام به قبل أن تصبح كريسبر علاجًا روتينيًا لأمراض القلب. تحتاج الأبحاث إلى التغلب على التحديات المرتبطة بالسلامة والدقة في التعديل الجيني. بالإضافة إلى ذلك، يجب أن تستمر المناقشات الأخلاقية لضمان استخدام هذه التقنية بشكل مسؤول ومفيد. مستقبل كريسبر يحمل إمكانيات كبيرة، لكن تحقيق هذه الإمكانيات يتطلب تضافر الجهود العلمية والأخلاقية والاجتماعية.
⭐ مقالات قد تهمك
← علاج أمراض القلب بناءً على البصمة الوراثية
← دور الذكاء الاصطناعي في تشخيص أمراض القلب
← أحدث الدراسات حول العلاقة بين النظام الغذائي وأمراض القلب
← تقنيات التصوير المتقدمة للكشف المبكر عن أمراض القلب
← أثر التلوث البيئي على صحة القلب وكيفية الوقاية
← استخدام الطباعة ثلاثية الأبعاد في تصنيع الأنسجة والأعضاء القلبية
← علاج فشل القلب باستخدام الخلايا الجذعية
← استخدام الجراحة الروبوتية في عمليات القلب الدقيقة
← الجراحة بمساعدة الروبوت: هل هي المستقبل لجراحة القلب المفتوح؟
← الجيل الجديد من صمامات القلب القابلة للزرع
✦ تعرف على جراحات القلب الدقيقة مع دكتور ياسر النحاس
← تغيير الصمام الميترالي بالمنظار
😟 قلقان؟؟ ابعتلنا سؤالك او كلمنا وهنرد عليك على طول
⬇
🩺 اسأل دكتور ياسر النحاس
عندك سؤال عن عملية القلب المفتوح أو جراحة القلب بالمنظار أو عملية القلب النابض؟ ابعت سؤالك وسنرد عليك بشكل واضح وبسيط.
⏱️ يُفضّل كتابة: العمر + التشخيص إن وُجد + الأعراض + أي عمليات أو قسطرة سابقة + الأدوية الحالية.
تجارب المرضى الأعزاء